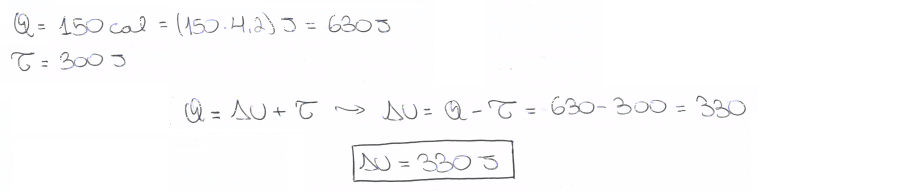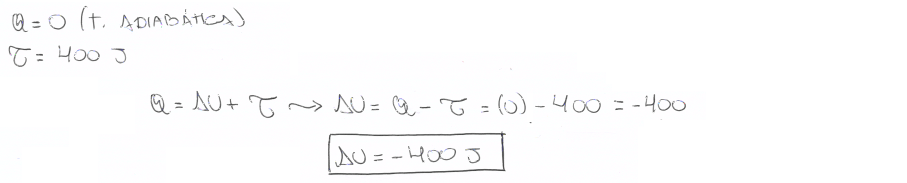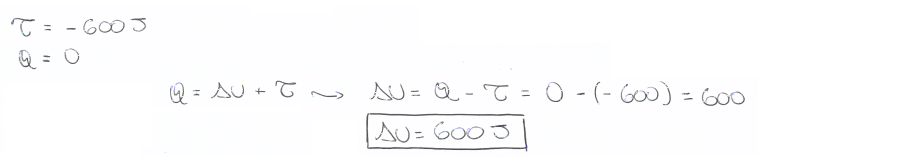Lista
Lista 
Lista 6-48: Leis da termodinâmica

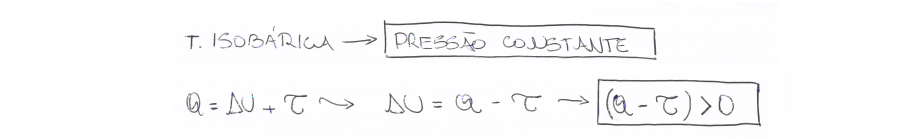
01. Em uma transformação isobárica, a pressão do gás é _______, e sua energia interna aumenta se a diferença entre ______ e _______ for _________.
|
a) constante, calor, trabalho, nula. b) constante, calor, trabalho, negativa. c) variável, calor, trabalho, positiva. |
d) constante, trabalho, calor, negativa. e) constante, calor, trabalho, positiva. |
02. Um gás é submetido a um processo sob pressão constante de 400 N/m2 e sofre uma redução de seu volume em 0,25 m3. Assinale aquilo que for FALSO:
a) a quantidade de trabalho realizada sobre o gás foi de - 100 J.
b) a variação da energia interna é de -150 J.
c) o gás recebe 250 J de calor.
d) o gás cede 250 J de calor.
e) a variação de temperatura desse gás é negativa.
03. Sobre os gases monoatômicos e ideais que passam por um processo de transformação isobárica, podemos afirmar corretamente que:
a) Toda a quantidade de calor (Q) cedida ao sistema será transformada em trabalho mecânico.
b) A quantidade de calor (Q) cedida ao sistema é diretamente proporcional à sua variação de temperatura.
c) A energia interna do gás (U) permanece constante.
d) A variação de energia interna(ΔU) é inversamente proporcional à variação volumétrica (ΔV).
e) A temperatura do gás varia, mas não há trocas de calor entre o sistema e o meio externo.
04. Um gás ideal sofre uma transformação: absorve 150 cal de energia na forma de calor e expande-se, realizando um trabalho de 300 J. Considerando 1 cal = 4,2 J, a variação da energia interna do gás (ΔU) é, em J:
|
a) 250. b) 350. |
c) 500. d) 330. |
e) 900. |
05. Um gás monoatômico e ideal sofre uma expansão adiabática, realizando sobre um pistão um trabalho termodinâmico igual a 400 J. Qual é a variação da energia interna do gás, em joules?
|
a) -400 J. b) 400 J. |
c) 200 J. d) -200 J. |
e) -100 J. |
06. Um pistão comprime um gás, realizando um trabalho de 600 J sobre ele. Considerando que o pistão não permite a troca de calor entre o gás e o meio externo e que a transformação ocorreu muito rapidamente, indique a variação da energia interna sofrida pelo gás:
|
a) -600 J. b) 300 J. |
c) -200 J. d) 600 J. |
e) -300 J. |
07. (VUNESP-UNESP) Dois copos de vidro iguais, em equilíbrio térmico com a temperatura ambiente, foram guardados, um dentro do outro, conforme mostra a figura. Uma pessoa, ao tentar desencaixá-los, não obteve sucesso. Para separá-los, resolveu colocar em prática seus conhecimentos da física térmica.

De acordo com a física térmica, o único procedimento capaz de separá-los é:
a) mergulhar o copo B em água em equilíbrio térmico com cubos de gelo e encher o copo A com água à temperatura ambiente.
b) colocar água quente (superior à temperatura ambiente) no copo A.
c) mergulhar o copo B em água gelada (inferior à temperatura ambiente) e deixar o copo A sem líquido.
d) encher o copo A com água quente (superior à temperatura ambiente) e mergulhar o copo B em água gelada (inferior à temperatura ambiente).
e) encher o copo A com água gelada (inferior à temperatura ambiente) e mergulhar o copo B em água quente (superior à temperatura ambiente).
08. (UFRGS 2017) Observe a figura abaixo.
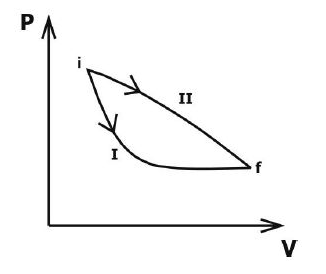
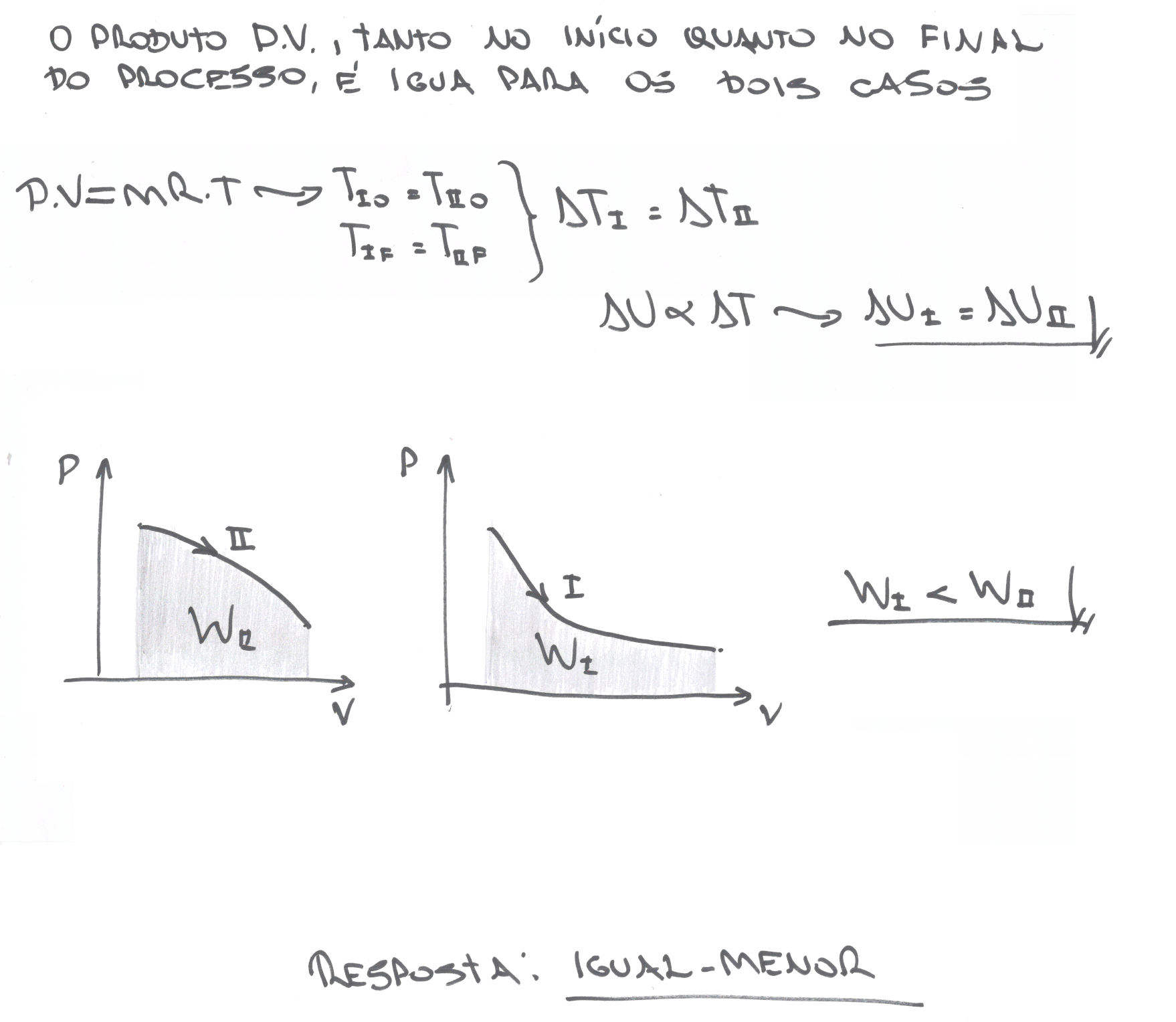
A figura mostra dois processos, I e II, em um diagrama pressão (P) x volume (V) ao longo dos quais um gás ideal pode ser levado do estado inicial i para o estado final f.
Assinale a alternativa que preenche corretamente as lacunas do enunciado abaixo, na ordem em que aparecem.
De acordo com a 1ª Lei da Termodinâmica, a variação da energia interna é ........ nos dois processos. O trabalho WI realizado no processo I é ........ que o trabalho WII realizado no processo II.
|
a) igual - maior. b) igual - menor. |
c) igual - igual. d) diferente - maior. |
e) diferente - menor. |
09. (URCA 2017/1) Considere o texto:
Um conceito amplo de calor se refere a forma de transferência de energia não mecânica entre sistema e vizinhança, ou seja, uma forma de transferência de energia entre sistema e vizinhança não relacionada a trabalho mecânico, podendo ser decorrente de diferença de temperatura entre sistema e vizinhança ou mesmo advinda de radiação solar etc.
Podemos dizer que se um sistema termodinâmico libera para a vizinhança, num certo processo, uma quantidade de calor cujo valor absoluto é 7 joules e realiza um trabalho de 3 joules então, de acordo com a primeira lei da termodinâmica, a variação de energia interna do sistema, é:
|
a) 10 joules. b) -10 joules. |
c) 4 joules. d) -4 joules. |
e) 2 joules. |
10. (URCA 2017/1) De acordo com a primeira lei da termodinâmica se, durante um processo isotérmico sofrido por um gás ideal de massa fixa, o gás libera uma quantidade de calor cujo módulo é de 50cal então a variação de energia interna e o trabalho realizado pelo gás neste processo são, respectivamente:
|
a) 0 e 50 cal. b) 50 cal e 0. |
c) 0 e 0. d) 50 cal e -50 cal. |
e) 0 e -10 cal. |
11. (URCA 2016/2) Considere o texto:
"Um conceito amplo de calor se refere a forma de transferência de energia não mecânica entre sistema e vizinhança, ou seja, uma forma de transferência de energia entre sistema e vizinhança não relacionada a trabalho mecânico, podendo ser decorrente de diferença de temperatura entre sistema e vizinhança ou mesmo advinda de radiação solar etc."
Levando em consideração o texto apresentado acima, podemos dizer que se a terra recebe uma quantidade de energia Q do sol, então considerando que não há trabalho realizado sobre a terra nem por ela, a variação de energia interna da terra neste processo é, de acordo com a primeira lei da termodinâmica:
a) ΔU = Q, que corresponde ao calor por radiação recebido do sol.
b) ΔU = 0.
c) ΔU = Q/3.
d) ΔU = 2Q.
e) ΔU = Q/2.
12. Certo gás diatômico e ideal recebe 12 J de calor de uma fonte externa durante uma transformação isocórica. Considerando que o gás não cede qualquer quantidade de energia em forma de calor para suas vizinhanças, a variação da energia interna do gás, durante essa transformação, é de:
|
a) 6 J. b) -12 J. |
c) 12 J. d) 24 J. |
e) -24. |
13. Durante um processo isovolumétrico, um gás recebe do meio externo uma quantidade de calor Q. Podemos afirmar que a variação de sua energia interna e sua pressão terão seus módulos, respectivamente:
a) Mantido constante e aumentado
b) Reduzido e aumentado
c) Aumentado e aumentado
d) Reduzido e mantido constante
e) Aumentado e reduzido